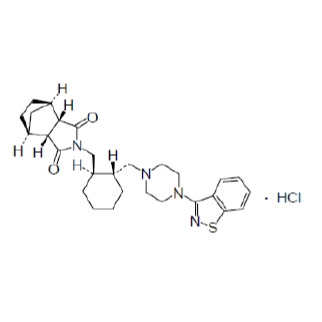
(→化学结构) |
无编辑摘要 |
||
| 第35行: | 第35行: | ||
== 不良反应 == | == 不良反应 == | ||
以下内容来自本品美国说明书中【不良反应】信息,尚缺乏中国患者应用本品超过80 mg/日剂量的安全有效性证据。 | |||
鲁拉西酮(20-160 mg/日)治疗精神分裂症的短期、安慰剂对照的上市前研究(n=1508)发现下述不良反应: | |||
常见的不良反应(发生率≥5%且至少是安慰剂组的两倍):嗜睡、静坐不能、锥体外系症状和恶心。 | |||
导致治疗中止的不良反应:总计9.5%(143/1508)的鲁拉西酮组患者和9.3%(66/708)的安慰剂组患者由于不良反应而停药。鲁拉西酮组中没有观察到导致治疗中止的、发生率至少为2%且至少为安慰剂组两倍的不良反应。 | |||
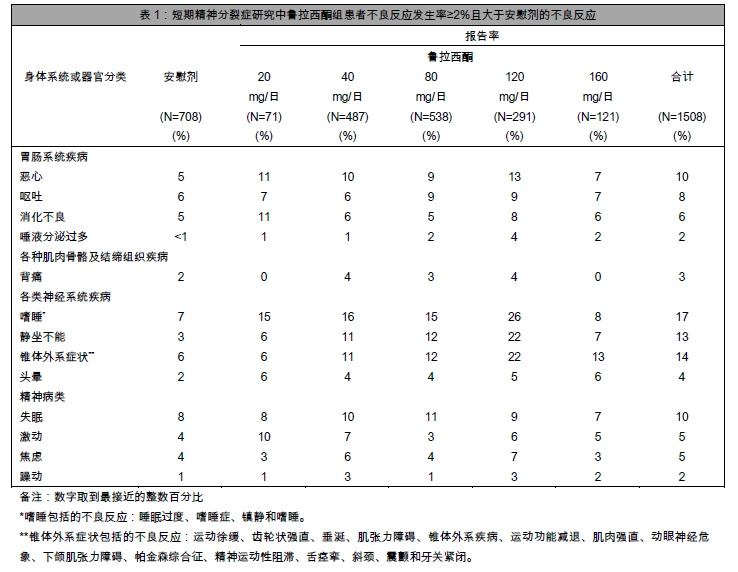
接受鲁拉西酮治疗的患者中发生率≥2%的不良反应:在急性治疗期间(精神分裂症患者接受治疗最长至6周)发生的与鲁拉西酮用药相关的不良反应(发生率(取到最接近的整数百分比)≥2%,且鲁拉西酮组的发生率高于安慰剂组)如下表所示。 | |||
[[File:Latuda Adverse Reaction.jpg]] | [[File:Latuda Adverse Reaction.jpg]] | ||
2022年3月20日 (日) 18:45的版本
鲁拉西酮是一新型非典型抗精神病药物,商品名为罗舒达(Latuda),主要用于治疗双相情感障碍I型抑郁发作和精神分裂症。
化学结构
分子式:C28H36N4O2S·HCl
分子量:529.14
警示语
增加患有痴呆相关性精神病的老年患者的死亡率。
与安慰剂相比,使用非典型抗精神病药治疗患有痴呆相关性精神病的老年患者时,死亡的风险会增加。对在患有痴呆相关精神病的老年患者中进行的17项安慰剂对照临床试验(平均众数治疗时间为10周)的分析发现,药物治疗组患者死亡的危险性为安慰剂对照组的1.6-1.7倍。在一项10周对照临床试验中,药物治疗组的死亡率为4.5%,安慰剂对照组为2.6%。虽然死亡原因各异,但是大多数死于心血管病(如心衰、猝死)或感染(如肺炎)。研究显示,与非典型抗精神病药物相似,采用传统抗精神病药物治疗可能增加死亡率。观察研究中死亡率的增加归因于抗精神病药物还是患者本身的某些特性造成的,目前尚不清楚。鲁拉西酮未被批准用于治疗痴呆相关的精神病患者。
性质
本品为白色或类白色圆形薄膜衣片,单面刻有“L40”字样。
用法用量
一般成人的初始剂量为每次40 mg,每日一次,初始剂量不需要进行滴定。根据症状可增加到每次80mg,每日一次。本品应与食物(至少350千卡)同服。 本品在中国成人精神分裂症患者中开展的随机对照临床试验仅验证了最高剂量80 mg/日的安全有效性,尚缺乏中国患者应用本品超过80 mg/日剂量的安全有效性证据。
尚未在对照研究中明确鲁拉西酮超过6周的长期治疗有效性。因此,医生在选择使用鲁拉西酮进行较长时间治疗时,应定期对药物在患者中的长期有效性进行再评价。
中度(肌酐清除率:30-<50 mL/min)和重度(肌酐清除率:<30 mL/min)肾损害患者的初始剂量推荐为20 mg/日。最大剂量为每次80mg,每日一次。 中度(Child-Pugh评分=7-9)和重度(Child-Pugh评分=10-15)肝损伤患者的初始剂量推荐为20 mg/日。中度肝损伤患者的最大剂量为每次80 mg,每日一次,重度肝损伤患者为每次40 mg,每日一次。
与CYP3A4中效抑制剂(如地尔硫䓬)合用时,初始剂量应减半。最大剂量为每次80 mg,每日一次。
由于葡萄柚和葡萄柚汁可能会抑制CYP3A4而改变鲁拉西酮的浓度,服用鲁拉西酮的患者应避免食用葡萄柚和葡萄柚汁。
与CYP3A4中效诱导剂合用时,可能有必要在与CYP3A4诱导剂治疗一段时间(7天或更长)后增加鲁拉西酮剂量。
禁忌
本品不应和CYP3A4强效抑制剂(如:酮康唑、克拉霉素、利托那韦、伏立康唑、米贝拉地尔)和强效诱导剂(如:利福平、阿伐麦布、圣约翰草、笨妥英、卡马西平等)合用。
不良反应
以下内容来自本品美国说明书中【不良反应】信息,尚缺乏中国患者应用本品超过80 mg/日剂量的安全有效性证据。
鲁拉西酮(20-160 mg/日)治疗精神分裂症的短期、安慰剂对照的上市前研究(n=1508)发现下述不良反应:
常见的不良反应(发生率≥5%且至少是安慰剂组的两倍):嗜睡、静坐不能、锥体外系症状和恶心。
导致治疗中止的不良反应:总计9.5%(143/1508)的鲁拉西酮组患者和9.3%(66/708)的安慰剂组患者由于不良反应而停药。鲁拉西酮组中没有观察到导致治疗中止的、发生率至少为2%且至少为安慰剂组两倍的不良反应。
接受鲁拉西酮治疗的患者中发生率≥2%的不良反应:在急性治疗期间(精神分裂症患者接受治疗最长至6周)发生的与鲁拉西酮用药相关的不良反应(发生率(取到最接近的整数百分比)≥2%,且鲁拉西酮组的发生率高于安慰剂组)如下表所示。