氨基酸是一种两性生物小分子,其化学定义是含有氨基的取代羧酸。
分类
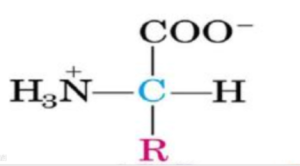
生物体内有多种氨基酸,通常情况下我们说的氨基酸指蛋白质的单体小分子,即α氨基酸,其分子中羧基与氨基位于同一个碳原子上,这个碳原子称为α-碳原子,α-碳原子上的另外两个基团分别是氢原子和-R基团(即侧链基团),侧链基团不同决定氨基酸的命名与特性。
将氨基酸的主链进行编号(化学中通常选用希腊字母进行依次编号),其中与羧基直接相连的碳原子称为α-碳原子,沿主链向下,分别是β-碳原子,γ-碳原子等,按照氨基位置分别命名为β-氨基酸,γ-氨基酸等。其序列可参考希腊字母表序列进行依次编号命名。在生物体内,除α氨基酸之外,其他氨基酸也可以参与生命活动,在生物代谢中具有重要作用。
按照氨基酸的酸碱性(即羧基和氨基的比例)可以将氨基酸分为酸性氨基酸,碱性氨基酸和中性氨基酸等三类。其中,酸性氨基酸是因为分子中羧基多于氨基,在氨基接受羧基解离的氢离子之后仍有剩余氢离子,所以呈酸性;碱性氨基酸中,氨基多于羧基,在接受羧基电离出的氢离子之后仍有孤电子对能够继续接受氢离子形成配位键,故水溶液显碱性。α-氨基酸中,典型的酸性氨基酸有谷氨酸(分子中的两个羧基呈现酸性),典型的碱性氨基酸有色氨酸(分子中咪唑基与α-氨基共同作用呈现碱性)。
典型结构
生物体内能够形成蛋白质的氨基酸均为α氨基酸,即羧基与氨基位于同一个碳原子上。除最简单的甘氨酸(侧链基团为氢原子)之外,其余氨基酸的α碳原子上均连接4个不同基团,导致其具有手性与旋光性,即其不同构型的氨基酸水溶液与晶体会导致偏振光朝不同方向进行偏转。生物体内的氨基酸均为L型氨基酸,但是D型氨基酸形成的多肽链在最终形成蛋白质之后也会有生物学活性,故生物体内自行合成L型氨基酸可能是偶然选择的结果。
蛋白质中氨基酸的差异出现在其侧链基团(-R基),R-基的结构决定了氨基酸的特殊性质以及特殊的生理活性,如可以作为神经递质或者是作为激素进行生物信号的传递,或者是在代谢过程中进行调控等作用。通常情况下我们讨论的氨基酸的结构即为其-R基团的结构。
在所有α-氨基酸中有一个特例,即脯氨酸,其有机化学命名法下的名称是:β-吡咯烷基-α-羧酸,这是所有α-氨基酸中唯一一个亚氨基酸,其亚氨基位于结构中的吡咯烷基中,不存在完整的氨基结构。
通性
手性
除甘氨酸之外,所有α-氨基酸(蛋白质氨基酸)的α碳原子上都连接了4个不同的基团(氨基,羧基,氢原子以及侧链基团-R),这种结构会给分子带来旋光性和两种不同的旋光结构,其化学性质没有明显差异但是在物理性质上会带来熔沸点以及旋光性的差异,详情请参考站内手性化合物相关连接。
酸碱性
因为氨基酸分子中同时含有氨基与羧基,这意味着氨基酸在给出氢离子的同时还具有给出孤电子对的能力,即氨基酸同时具有酸性和碱性。但是因为羧基电离的不完全性以及孤电子对接受电子的能力限制,氨基酸同时具有的是弱酸性和弱碱性,且受到分子内超共轭效应以及电子效应影响,不同氨基酸的电离常数有一定的差异。
氨基酸的解离遵循弱电解质的电离平衡规律,其具有一级解离和二级解离两级,在酸性条件下的一级解离是让电离的羧酸根离子重新生成羧基结构即生成有机酸结构形式,酸性条件下的二级电离是将氨基结合形成铵盐;碱性条件下的两步电离与酸性条件下的电离恰好相反。两步电离均具有相应的平衡常数,可以根据平衡常数衡量两次电离的强度。
α-羧基参与的反应
主要是酯化反应,酰化反应等,详细信息请参考有机化学相关页面。
α-氨基参与的反应
游离α-氨基可以被酰氯或者酸酐酰化,酰氯和酸酐是蛋白质人工合成过程中的氨基保护剂。也可以被烃化剂烃化,常用烃化剂通常有2,4-二硝基氟苯或者苯异硫氰酸酯。
α-羧基与α-氨基共同参与的反应
成肽反应
一个氨基酸的氨基与另一个氨基酸的羧基可以发生脱水缩合形成肽键,这种反应称为成肽反应。在生物体内有复杂的酶系进行催化反应,在体外通常使用乙二醇进行催化反应,可以生成一定结构的肽链。
茚三酮反应
茚三酮是一种强氧化剂,在弱酸性溶液中可以与α-氨基酸共热引发氧化脱氨基反应,产生的氨,还原茚三酮与另一个茚三酮分子结合产生紫色物质,这种紫色物质可以在570nm进行定量测定。
旋光性以及光谱性质
除甘氨酸外的所有α-氨基酸均为手性分子,故具有一定的旋光性,其手性中心均为其α碳原子。苏氨酸和异亮氨酸具有两个手性中心,除α-碳之外有另一个手性碳原子,所有其具有4种手性结构。
所有蛋白质氨基酸在可见光区均无明显吸收峰,但是在红外区和远紫外区均有明显吸收峰,芳香族氨基酸在近紫外区具有一定的吸收峰,其原因在于其侧链基团含有共轭π键。
生物学功能
除合成蛋白质之外,氨基酸还有相当多其他生物学功能,如在神经系统中作为神经递质(谷氨酸等)或者是作为激素进行信号传递。
参考资料
- 朱圣庚 徐长法《生物化学》第四版上册